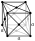Содержание
| Никель является жарпочрочным, жаростойким и коррозионностойким металлом, что определяет его применение в качестве конструкционного материала для изделий, подверженных воздействию различных агрессивных сред в том числе при повышенных температурах, а также подверженных механическим нагрузкам при высоких температурах. Помимо этого никель служит является популярным легирующим элементом для сталей и сплавов. На странице представлено описание данного металла: физические свойства, области применения, марки никеля, виды продукции. |
Основные сведения о никеле
Никель (Ni) (Niccolum) — химический элемент с атомным номером 28 в периодической системе, ковкий и пластичный металл. Имеет серебристый цвет с желтоватым оттенком, хорошо полируется, притягивается магнитом. Плотность никеля составляет 8,902 г/см 3 , температура плавления tпл. = 1453°С, температура кипения tкип. = 2730-2915°С, данный металл является ферромагнетиком, точка Кюри около 358 °C. На воздухе компактный никель стабилен. Поверхность никеля покрыта тонкой пленкой оксида NiO, которая прочно предохраняет металл от дальнейшего окисления.
В земной коре содержание никеля составляет около 8·10 -3 % по массе. Возможно, громадные количества никеля — около 17·10 19 тонн — заключены в ядре Земли, которое, по одной из распространенных гипотез, состоит из железоникелевого сплава. В морской воде содержание никеля составляет примерно 1·10 -8 -5·10 -8 %.
История открытия никеля
Свойства никеля
Физические свойства никеля
| Свойство | Никель |
|---|---|
| Атомный номер | 28 |
| Атомная масса, а.е.м | 58,69 |
| Атомный диаметр, пм | 248 |
| Плотность, г/см³ | 8,902 |
| Удельная теплоемкость, Дж/(K·моль) | 0,443 |
| Теплопроводность, Вт/(м·K) | 90,9 |
| Температура плавления, °С | 1453 |
| Температура кипения, °С | 2730-2915 |
| Теплота плавления, кДж/моль | 17,61 |
| Теплота испарения, кДж/моль | 378,6 |
| Молярный объем, см³/моль | 6,6 |
| Группа металлов | Тяжелый металл |
Химические свойства никеля
| Свойство | Никель |
|---|---|
| Ковалентный радиус, пм | 115 |
| Радиус иона, пм | (+2e) 69 |
| Электроотрицательность (по Полингу): | 1,91 |
| Электродный потенциал: | 0 |
| Степени окисления: | 3, 2, 0 |
Марки никеля и сплавов
Достоинства / недостатки никеля
-
Достоинства:
- обладает высокой жаропрочностью и жаростойкостью;
- имеет высокую коррозионную стойкость во многих агрессивных средах.
-
Недостатки:
- имеет высокую стоимость.
Применение никеля
Никель по большей части является составным компонентом различных сплавов. Все нержавеющие стали обязательно содержат никель, так как никель повышает химическую стойкость сплава. Также сплавы никеля характеризуются высокой вязкостью и используются при изготовлении прочной брони. При изготовлении важнейших деталей различных приборов используется сплав никеля с железом (36-38% никеля), обладающий низким коэффициентом термического расширения.
При изготовлении сердечников электромагнитов широкое применение находят сплавы под общим названием пермаллои. Эти сплавы, кроме железа, содержат от 40 до 80% никеля. Из никелевых сплавов чеканятся монеты. Общее число различных сплавов никеля, находящих практическое применение, достигает нескольких тысяч.
Различные металлы никелируют, что позволяет защитить их от коррозии. На металл наносится тонкий никелевый слой, обладающий высокой коррозионной стойкостью. Вместе с этим никелирование придает изделиям красивый внешний вид.
Никель широко используют при изготовлении различной химической аппаратуры, в кораблестроении, в электротехнике, при изготовлении щелочных аккумуляторов, для многих других целей. Специально приготовленный дисперсный никель находит широкое применение как катализатор самых разных химических реакций. Оксиды никеля используют при производстве ферритных материалов и как пигмент для стекла, глазурей и керамики; оксиды и некоторые соли служат катализаторами различных процессов. Производство железо-никелевых, никель-кадмиевых, никель-цинковых, никель-водородных аккумуляторов.
| Никель | |
|---|---|
| ← Кобальт | Медь → | |
| 28 | Ni ↓ Pd |

(молярная масса)
(первый электрон)
Ни́кель — химический элемент десятой (по устаревшей короткопериодной форме — восьмой) группы, четвёртого периода периодической системы, с атомным номером 28. Обозначается символом Ni (лат. Niccolum ). Простое вещество никель — это пластичный, ковкий, переходный металл серебристо-белого цвета, при обычных температурах на воздухе покрывается тонкой плёнкой оксида. Химически малоактивен.
Содержание
Происхождение названия [ править | править код ]
Элемент получил своё название от имени духа гор (ср. нем. Nickel — озорник) немецкой мифологии, который «подбрасывал» искателям меди минерал красного цвета, похожий на медную руду (ныне известный как никелин).
История [ править | править код ]
Никель (англ., франц. и нем. Nickel) открыт в 1751 г. Однако задолго до этого саксонские горняки хорошо знали руду, которая внешне походила на медную и применялась в стекловарении для окраски стёкол в зелёный цвет. Все попытки получить из этой руды медь оказались неудачными, в связи с чем в конце XVII в. руда получила название купферникель (Kupfernickel), что переводится как «Медный упрямец» или «Медный озорник». Данную руду (красный никелевый колчедан NiAs) в 1751 г. исследовал шведский минералог А. Кронстедт. Ему удалось получить зелёный окисел и путём восстановления последнего — новый металл, названный никелем. Когда Бергман получил металл в более чистом виде, он установил, что по своим свойствам металл похож на железо; более подробно никель изучали многие химики, начиная с Пруста. Никкел — ругательное слово на языке горняков. Оно образовалось из искажённого Nicolaus — родового слова, имевшего несколько значений. Но главным образом слово Nicolaus служило для характеристики двуличных людей; кроме того, оно обозначало «озорной маленький дух», «обманчивый бездельник» и т. д. В русской литературе начала XIX в. употреблялись названия николан (Шерер, 1808 и Захаров, 1810), николь и никель (Двигубский, 1824).
Физические свойства [ править | править код ]
Никель — серебристо-белый металл, не тускнеет на воздухе. Имеет гранецентрированную кубическую решетку с периодом a = 0,35238 нм, пространственная группа Fm3m. В чистом виде весьма пластичен и поддается обработке давлением. Является ферромагнетиком с точкой Кюри 358 °C.
Химические свойства [ править | править код ]
.</p>
<p>Никель образует соединения со степенью окисления +1, +2, +3 и +4. При этом соединения никеля со степенью окисления +4 редкие и неустойчивые [4] . Оксид никеля Ni<sub>2</sub>O<sub>3</sub> является сильным окислителем.</p>
<p>Никель характеризуется высокой коррозионной стойкостью — устойчив на воздухе, в воде, в щелочах, в ряде кислот [5] . Химическая стойкость обусловлена его склонностью к пассивированию — образованию на его поверхности плотной оксидной плёнки, обладающей защитным действием. Никель активно растворяется в разбавленной азотной кислоте:</p>
<p style=)
ightarrow 3Ni(NO_<3>)_<2>+2NO+4H_<2>O>>>
и в горячей концентрированной серной:
N i + 2 H 2 S O 4 → N i S O 4 + S O 2 + 2 H 2 O
ightarrow NiSO_<4>+SO_<2>+2H_<2>O>>>
С соляной и с разбавленной серной кислотами реакция протекает медленно. Концентрированная азотная кислота пассивирует никель, однако при нагревании реакция всё же протекает [6] (основной продукт восстановления азота — NO2).
С оксидом углерода CO никель легко образует летучий и очень ядовитый карбонил Ni(CO)4.
Тонкодисперсный порошок никеля пирофорный (самовоспламеняется на воздухе).
Никель горит только в виде порошка. Образует два оксида NiO и Ni2O3 и соответственно два гидроксида Ni(OH)2 и Ni(OH)3. Важнейшие растворимые соли никеля — ацетат, хлорид, нитрат и сульфат. Водные растворы солей окрашены обычно в зелёный цвет, а безводные соли — жёлтые или коричнево-жёлтые. К нерастворимым солям относятся оксалат и фосфат (зелёные), три сульфида: NiS (черный), Ni3S2 (желтовато-бронзовый) и Ni3S4 (серебристо-белый). Никель также образует многочисленные координационные и комплексные соединения. Например, диметилглиоксимат никеля Ni(C4H6N2O2)2, дающий чёткую красную окраску в кислой среде, широко используется в качественном анализе для обнаружения никеля.

Водные растворы солей никеля(II) содержат ион гексаакваникеля(II) [Ni(H2O)6] 2+ . При добавлении к раствору, содержащему эти ионы, аммиачного раствора происходит осаждение гидроксида никеля (II), зелёного желатинообразного вещества. Этот осадок растворяется при добавлении избыточного количества аммиака вследствие образования ионов гексааминникеля(II) [Ni(NH3)6] 2+ .
Никель образует комплексы с тетраэдрической и с плоской квадратной структурой. Например, комплекс тетрахлороникелат (II) [NiCl4] 2− имеет тетраэдрическую структуру, а комплекс тетрацианоникелат(II) [Ni(CN)4] 2− имеет плоскую квадратную структуру.
В качественном и количественном анализе для обнаружения ионов никеля (II) используется щелочной раствор бутандиондиоксима, известного также под названиями диметилглиоксим и реактив Чугаева. То, что это вещество является реактивом на никель, установил в 1905 году Л. А. Чугаев [7] [8] . При его взаимодействии с ионами никеля (II) образуется красное координационное соединение бис(бутандиондиоксимато)никель(II). Это — хелатное соединение, и бутандиондиоксимато-лиганд является бидентатным.
Нахождение в природе [ править | править код ]
Никель довольно распространён в природе — его содержание в земной коре составляет ок. 0,01 %(масс.). В земной коре встречается только в связанном виде, в железных метеоритах содержится самородный никель (от 5 до 25 %). Содержание его в ультраосновных породах примерно в 200 раз выше, чем в кислых (1,2 кг/т и 8г/т). В ультраосновных породах преобладающее количество никеля связано с оливинами, содержащими 0,13—0,41 % Ni. Он изоморфно замещает железо и магний. Небольшая часть никеля присутствует в виде сульфидов. Никель проявляет сидерофильные и халькофильные свойства. При повышенном содержании в магме серы возникают сульфиды никеля вместе с медью, кобальтом, железом и платиноидами. В гидротермальном процессе совместно с кобальтом, мышьяком и серой и иногда с висмутом, ураном и серебром, никель образует повышенные концентрации в виде арсенидов и сульфидов никеля. Никель обычно содержится в сульфидных и мышьяк-содержащих медно-никелевых рудах.
- никелин (красный никелевый колчедан, купферникель) NiAs
- хлоантит (белый никелевый колчедан) (Ni, Co, Fe)As2
- гарниерит (Mg, Ni)6(Si4O11)(OH)6·H2O и другие силикаты
- магнитный колчедан (Fe, Ni, Cu)S
- мышьяково-никелевый блеск (герсдорфит) NiAsS,
- пентландит (Fe,Ni)9S8
В растениях в среднем 5⋅10 −5 весовых процентов никеля, в морских животных — 1,6⋅10 −4 , в наземных — 1⋅10 −6 , в человеческом организме — 1,2⋅10 −6 . О никеле в организмах известно уже немало. Установлено, например, что содержание его в крови человека меняется с возрастом, что у животных количество никеля в организме повышено, наконец, что существуют некоторые растения и микроорганизмы — «концентраторы» никеля, содержащие в тысячи и даже в сотни тысяч раз больше никеля, чем окружающая среда.
Месторождения никелевых руд [ править | править код ]
Основные месторождения никелевых руд находятся в Канаде, России (Мурманская область, Норильский район, Урал, Воронежская область [9] ), Кубе, ЮАР, Албании, Греции, а также на Новой Каледонии и Украине [10] .
Наибольшими запасами никеля в мире обладает Индонезия (21 млн тонн). Там добывается больше всего никеля в год (более 340 тыс. тонн) [11] .
Природные изотопы никеля [ править | править код ]
Природный никель содержит 5 стабильных изотопов: 58 Ni (68,27 %), 60 Ni (26,10 %), 61 Ni (1,13 %), 62 Ni (3,59 %), 64 Ni (0,91 %). Существуют также искусственно созданные изотопы никеля, самые стабильные из которых — 59 Ni (период полураспада 100 тысяч лет), 63 Ni (100 лет) и 56 Ni (6 суток).
Получение [ править | править код ]
Общие запасы никеля в рудах на начало 1998 года оцениваются в количестве 135 млн т., в том числе достоверные — 49 млн.т. Основные руды никеля — никелин (купферникель) NiAs, миллерит NiS, пентландит (FeNi)9S8 — содержат также мышьяк, железо и серу; в магматическом пирротине также встречаются включения пентландита. Другие руды, из которых тоже добывают Ni, содержат примеси Co, Cu, Fe и Mg. Иногда никель является основным продуктом процесса рафинирования, но чаще его получают как побочный продукт в технологиях других металлов. Из достоверных запасов, по разным данным, от 40 до 66 % никеля находится в «окисленных никелевых рудах» (ОНР), 33 % — в сульфидных, 0,7 % — в прочих. По состоянию на 1997 г. доля никеля, произведённого переработкой ОНР, составила порядка 40 % от общемирового объёма производства. В промышленных условиях ОНР делят на два типа: магнезиальные и железистые.
Тугоплавкие магнезиальные руды, как правило, подвергают электроплавке на ферроникель (5—50 % Ni+Co, в зависимости от состава сырья и технологических особенностей).
Наиболее железистые — латеритовые руды перерабатывают гидрометаллургическими методами с применением аммиачно-карбонатного выщелачивания или сернокислотного автоклавного выщелачивания. В зависимости от состава сырья и применяемых технологических схем конечными продуктами этих технологий являются: закись никеля (76-90 % Ni), синтер (89 % Ni), сульфидные концентраты различного состава, а также металлические никель электролитный, никелевые порошки и кобальт.
Менее железистые — нонтронитовые руды плавят на штейн. На предприятиях, работающих по полному циклу, дальнейшая схема переработки включает конвертирование, обжиг файнштейна, электроплавку закиси никеля с получением металлического никеля. Попутно извлекаемый кобальт выпускают в виде металла и/или солей. [12] Ещё один источник никеля: в золе углей Южного Уэльса в Англии — до 78 кг никеля на тонну. Повышенное содержание никеля в некоторых каменных углях, нефтях, сланцах говорит о возможности концентрации никеля ископаемым органическим веществом. Причины этого явления пока не выяснены.
«Никель долгое время не могли получить в пластичном виде вследствие того, что он всегда имеет небольшую примесь серы в форме сульфида никеля, расположенного тонкими, хрупкими прослойками на границах металла. Добавление к расплавленному никелю небольшого количества магния переводит серу в форму соединения с магнием, которое выделяется в виде зерен, не нарушая пластичности металла.» [13]
Основную массу никеля получают из гарниерита и магнитного колчедана.
- Силикатную руду восстанавливают угольной пылью во вращающихся трубчатых печах до железо-никелевых окатышей (5—8 % Ni), которые затем очищают от серы, прокаливают и обрабатывают раствором аммиака. После подкисления раствора из него электролитически получают металл.
- Карбонильный способ (метод Монда). Вначале из сульфидной руды получают медно-никелевый штейн, над которым пропускают СО под высоким давлением. Образуется легколетучий тетракарбонилникель [Ni(CO)4], термическим разложением которого выделяют особо чистый металл.
- Алюминотермический способ восстановления никеля из оксидной руды: 3NiO + 2Al = 3Ni +Al2O3
Применение [ править | править код ]
В 2015 году 67 % потребления никеля пришлось на производство нержавеющей стали, 17 % на сплавы без железа, 7 % на никелирование и 9 % на прочие применения, такие как аккумуляторы, порошковая металлургия и химические реактивы [14] .
Сплавы [ править | править код ]
Никель является основой большинства суперсплавов — жаропрочных материалов, применяемых в аэрокосмической промышленности для деталей силовых установок.
- монель-металл (65—67 % Ni + 30—32 % Cu + 1 % Mn), жаростойкий до 500 °C, очень коррозионно-устойчив;
- белое золото (например, 585 пробы содержит 58,5 % золота и сплав (лигатуру) из серебра и никеля (или палладия));
- нихром, сплав никеля и хрома (60 % Ni + 40 % Cr);
- пермаллой (76 % Ni + 17 %Fe + 5 % Cu + 2 % Cr), обладает высокой магнитной восприимчивостью при очень малых потерях на гистерезис;
- инвар (65 % Fe + 35 % Ni), почти не удлиняется при нагревании;
- Кроме того, к сплавам никеля относятся никелевые и хромоникелевые стали, нейзильбер и различные сплавы сопротивления типа константана, никелина и манганина. [15]
- Никель присутствует в качестве компонента ряда нержавеющих сталей.
Никелирование [ править | править код ]
Никелирование — создание никелевого покрытия на поверхности другого металла с целью предохранения его от коррозии. Проводится гальваническим способом с использованием электролитов, содержащих сульфат никеля(II), хлорид натрия, гидроксид бора, поверхностно-активные и глянцующие вещества, и растворимых никелевых анодов. Толщина получаемого никелевого слоя составляет 12—36 мкм. Устойчивость блеска поверхности может быть обеспечена последующим хромированием (толщина слоя хрома — 0,3 мкм).
Бестоковое никелирование проводится в растворе смеси хлорида никеля(II) и гипофосфита натрия в присутствии цитрата натрия:
N i C l 2 + N a H 2 P O 2 + H 2 O → N i + N a H 2 P O 3 + 2 H C l
ightarrow Ni+NaH_<2>PO_<3>+2HCl>>>
Процесс проводят при рН 4—6 и 95 °C [15] .
Производство аккумуляторов [ править | править код ]
Производство железо-никелевых, никель-кадмиевых, никель-цинковых, никель-водородных аккумуляторов.
Химическая технология [ править | править код ]
Радиационные технологии [ править | править код ]
Нуклид 63 Ni, излучающий β — -частицы, имеет период полураспада 100,1 года и применяется в крайтронах, а также детекторах электронного захвата (ЭЗД) в газовой хроматографии.
Медицина [ править | править код ]
- Применяется при изготовлении брекет-систем (никелид титана).
- Протезирование.
Монетное дело [ править | править код ]
Никель широко применяется при производстве монет во многих странах [16] . В США монета достоинством в 5 центов носит разговорное название «никель» [17] .
Музыкальная промышленность [ править | править код ]
Также никель используется для производства обмотки струн музыкальных инструментов.
Цены на никель [ править | править код ]
В течение 2012 года цены на никель колебались в пределах от $15 500 до $17 600 за тонну.
Биологическая роль [ править | править код ]

Никель относится к числу микроэлементов, необходимых для нормального развития живых организмов. Однако о его роли в живых организмах известно немного. Известно, что никель принимает участие в ферментативных реакциях у животных и растений. В организме животных он накапливается в ороговевших тканях, особенно в перьях. Повышенное содержание никеля в почвах приводят к эндемическим заболеваниям — у растений появляются уродливые формы, у животных — заболевания глаз, связанные с накоплением никеля в роговице. Токсическая доза (для крыс) — 50 мг. Особенно вредны летучие соединения никеля, в частности, его тетракарбонил Ni(CO)4. ПДК соединений никеля в воздухе составляет от 0,0002 до 0,001 мг/м 3 (для различных соединений).
Физиологическое действие [ править | править код ]

Никель и его соединения токсичны и канцерогенны.
Никель — основная причина аллергии (контактного дерматита) на металлы, контактирующие с кожей (украшения, часы, джинсовые заклепки). В 2008 году Американским обществом контактного дерматита никель был признан «Аллергеном года» [18] . В Европейском союзе ограничено содержание никеля в продукции, контактирующей с кожей человека [19] .
В XX веке было установлено, что поджелудочная железа очень богата никелем. При введении вслед за инсулином никеля продлевается действие инсулина и тем самым повышается гипогликемическая активность. Никель оказывает влияние на ферментативные процессы, окисление аскорбиновой кислоты, ускоряет переход сульфгидрильных групп в дисульфидные. Никель может угнетать действие адреналина и снижать артериальное давление. Избыточное поступление никеля в организм вызывает витилиго. Депонируется никель в поджелудочной и околощитовидной железах.
Никель и хром очень схожи по цвету. Более того некоторые мелкие производители фурнитуры присваивают эти названия одному и тому же цвету. Марки крупнее отличают никель от хрома.
В чем отличие никеля от хрома?
Как правило, никель это матовый цвет, он не отражает свет и не белстит на солнце. Хром – цвет блестящий, как привычный нам всем на сантехнике. Никель часто имеет немного желтоватый оттенок и смотрится не таким блестящим как хром.
Мы рекомендуем не погружаться в тонкости отличия этих цветов в теории и не ориентироваться на названия во избежание ошибки. Если вы хотите подобрать фурнитуру под какой либо цвет, уже существующий в вашем интерьере, то лучшим решением будет взять с собой в магазин образец и точно выбрать сочетания цветов визуально. Матовый никель сейчас очень популярен — он смотрится сдержанно и при этом очень дорого. Цвет не отражает от себя свет как хром и не создает световых ярких пятен, он подойдёт к интерьером как классического стиля так и hi tech.
«>