Наиболее часто сточные воды загрязнены минеральными кислотами: серной H2SO4, азотной HNO3, соляной HCl, а также их смесями. Значительно реже в сточных водах встречаются азотистая HNO2, фосфорная H3PO4, сернистая H2SO3, сероводородная H2S, плавиковая HF, хромовая H2СrO4 кислоты, а также органические кислоты: уксусная CH3COOH, пикриновая HOC6H2(NO2)3, угольная H2CO3, салициловая C6H4(OH)2 и др.
Сточные воды, содержащие минеральные кислоты или щелочи, перед сбросом их в водоемы или перед использованием в технологических процессах нейтрализуют. Практически нейтральными считаются воды, имеющие рН = 6,5-8,5.
Применяют следующие способы нейтрализации:
1) взаимная нейтрализация кислых и щелочных сточных вод смешением;
2) нейтрализация реагентами [растворы кислот, негашеная известь CaO, гашеная известь Ca(OH)2, кальцинированная сода Na2CO3, каустическая сода NaOH, аммиак NH4(ОH)];
3) фильтрование через нейтрализующие материалы [известь, известняк CaCO3, доломит CaCO3 · MgCO3, магнезит MgCO3, обожженный магнезит MgO, мел CaCO3 (96-99 %)];
4) нейтрализация дымовыми газами.
Нейтрализация сточных вод реагентами. Для нейтрализации кислых вод могут быть использованы: NaOH, KOH, Na2CO3 , NH4OH (аммиачная вода), CaCO3 , MgCO3 , цемент, доломит (CaCO3 · MgCO3). Однако наиболее дешевым является гидроксид кальция (известковое молоко) с содержанием активной извести Ca(OH)2 5-10 % (масс.). При гашении извести происходит ее гидратация с выделением теплоты:
Соду и гидроксид натрия следует использовать, если они являются отходами производства. Иногда для нейтрализации применяют различные отходы производства. Например, шлаки сталеплавильного, феррохромового и доменного производств используют для нейтрализации вод, содержащих серную кислоту.
Известь для нейтрализации вводят в сточную воду в виде гидроксида кальция – известкового молока – («мокрое» дозирование) или в виде сухого порошка («сухое» дозирование).
При нейтрализации производственных сточных вод, содержащих серную кислоту, реакция в зависимости от применяемого реагента протекает по уравнениям:
Поскольку в кислых и щелочных производственных сточных водах практически всегда присутствуют ионы металлов, то дозу регента следует определять с учетом выделения в осадок солей тяжелых металлов.
Количество реагентов G, кг/ч, для нейтрализации сточных вод определяется по формуле:
 (3.1)
(3.1)
где kз – коэффициент запаса расхода реагента по сравнению с теоретическим, равный для известкового молока 1,1, для известкового теста и сухой извести 1,5; В – количество активной части в товарном продукте, %; Q – расход сточных вод, подлежащих нейтрализации, м 3 /ч; а – расход реагента для нейтрализации, кг/кг; A – концентрация кислоты или щелочи, кг/м 3 .
При нейтрализации кислых сточных вод, содержащих соли тяжелых металлов, количество реагентов G, кг/ч, будет:
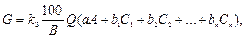 (3.2)
(3.2)
где С1 , С2 ,…, Сn – концентрации металлов в сточных водах, кг/м 3 ; b1 ,b2 ,…, bn – расход реагентов, требуемых для перевода металлов из растворенного состояния в осадок, кг/кг (табл. 3.3).
Объем осадка Voc, %, образующегося при нейтрализации 1 м 3 сточной воды, можно найти по уравнению:
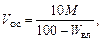 (3.3)
(3.3)
где Wвл – влажность осадка, %.
Нейтрализация кислых сточных вод в фильтрах с нейтрализующим материалом. Фильры применяют для нейтрализации кислых вод до концентрации кислот не более 1,5 мг/л в отсутствие в воде солей тяжелых металлов. В качестве загрузки используют: доломиты, известняк, магнезит, мел, мрамор и др. Размер кусков материала 3-8 см. Высоту загрузки Н для сточных вод, содержащих HCl и HNO3, принимают равной 1-1,5 м, а сдержащих H2SO4, – равной 1,5-2 м. Вода фильтруется сверху вниз или снизу вверх.
Нейтрализация дымовыми газами. Нейтрализация щелочных сточных вод газами, содержащих СO2, SO2, NO2, позволяет не только нейтрализовать сточные воды, но и одновременно осуществлять высокоэффективную очистку самих газов от вредных компонентов. Нейтрализация производится в реакторах с мешалкой или в колонной аппаратуре, расчет которых основан на закономерностях хемосорбции.
Не нашли то, что искали? Воспользуйтесь поиском:
Лучшие изречения: Как то на паре, один преподаватель сказал, когда лекция заканчивалась — это был конец пары: "Что-то тут концом пахнет". 8432 —  | 8045 —
| 8045 —  или читать все.
или читать все.
91.146.8.87 © studopedia.ru Не является автором материалов, которые размещены. Но предоставляет возможность бесплатного использования. Есть нарушение авторского права? Напишите нам | Обратная связь.
Отключите adBlock!
и обновите страницу (F5)
очень нужно
Читайте также:
- Биохимическая очистка сточных вод
- Измерение качественных параметров питьевых и сточных вод
- Местные установки для очистки и перекачки сточных вод
- Методы очистки сточных вод
- Нейтрализация цели
- Окисление загрязнителей сточных вод
- Отстаивание сточных вод
- Отстаивание сточных вод под действием центробежных сил
- Показатели качества сточных вод
- СЕКСУАЛЬНЫЙ АСПЕКТ КАББАЛЫ И ВОСТОЧНЫХ УЧЕНИЙ. ДОКТРИНА ЖЕНСТВЕННОГО
- Фильтрование сточных вод
Химическая очистка сточных вод
Нейтрализация смешением щелочных и кислых сточных вод.
Если щелочные и кислые сточные воды отводятся из различных производств или от различных предприятий отдельными потоками, то в качестве первой ступени их очистки рационально применить взаимную нейтрализацию. Нейтрализация щелочных и кислых сточных вод проводится в резервуарах-осреднителях при механическом перемешивании или при барботировании воздуха. Возможны два технологических варианта: непрерывная нейтрализация или нейтрализация с накоплением.
В первом случае потоки щелочных и кислых сточных вод подаются в резервуар непрерывно, также непрерывно нейтрализованная вода выводится из резервуара. Полнота нейтрализации обеспечивается автоматическим регулированием расходов щелочных и кислых вод. Во втором случае процесс нейтрализации осуществляется периодически.
Сначала в резервуар подается определенный объем кислых (или щелочных) сточных вод, а затем при перемешивании и непрерывном контроле величины рН постепенно добавляются щелочные (или кислые) сточные воды до полной нейтрализации. Нейтрализованная вода сливается, и процесс повторяется.
В обоих вариантах требуются дополнительные буферные резервуары для сброса избытка вод перед нейтрализацией, но первый вариант более сложен в обвязке и управлении.
Реагентная нейтрализация кислых сточных вод.
Нейтрализацию кислых сточных вод можно проводить различными химическими веществами основного характера: основными оксидами (негашеная известь CaO), гидроксидами (гашеная известь Ca(OH)2, каустическая сода NaOH, водный раствор аммиака NH4OH), солями слабых кислот, чаще всего карбонатами (кальцинированная сода Na2CO3, поташ K2CO3). Выбор реагента определяется только его доступностью и стоимостью. Наиболее распространенными реагентами являются гашеная и негашеная известь – продукт обжига известняка, сырье для производства силикатного кирпича, стекла, керамики и др. Гидроксид натрия или соду используют в том случае, если они сами являются отходами и их также необходимо утилизировать. Схема нейтрализации сточных вод известковым молоком показана на рис. 2.40.
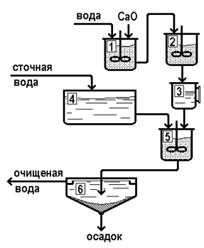
Рис. 2.40. Схема нейтрализации сточных вод известковым молоком
В аппарате для приготовления известкового молока 1 происходит измельчение и гашение оксида кальция:
Растворимость гидроксида кальция в воде при 25 0 С составляет около 1,5 г/л, поэтому большая часть гашеной извести образуется в виде суспензии. Образовавшаяся суспензия перекачивается насосом в растворные баки 2. Перемешивание в этих баках препятствует расслаиванию суспензии.
Сточная вода поступает в бак-осреднитель 4 и затем в нейтрализатор 5. Известковое молоко из растворных баков в необходимом количестве подается внейтрализатор 5 через мерник 3. Нейтрализованная сточная вода сливается в отстойник 6, в котором происходит отделение взвешенных частиц как присутствовавших в сырье (техническом оксиде кальция), так и образовавшихся в процессе нейтрализации, например при взаимодействии гидроокиси кальция с сульфат-ионами:
Помимо нейтрализации при небольшом избытке гидроокиси кальция происходит осаждение гидроокисей тяжелых металлов:
осадки которых отделяются известными способами.
Для нейтрализации кислых сточных вод вовсе не обязательно разлагать карбонат кальция и готовить известковое молоко. Карбонатсодержащие породы (известняк, мел, мрамор, доломит) можно использовать непосредственно, например, в составе фильтров-нейтрализаторов (рис. 2.41).
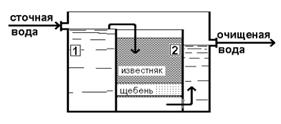
Рис. 2.41. Фильтр-нейтрализатор
Сточная вода подается в приемную камеру 1 для выравнивания расхода через фильтр, откуда переливом поступает в фильтровальную камеру 2, где и происходит нейтрализация:
При простоте конструкции фильтры-нейтрализаторы неприменимы для сточных вод, содержащих сульфат-ионы и ионы металлов, образующие труднорастворимые осадки из-за быстрого забивания каналов, увеличения сопротивления фильтра и его захлебывания.
Нейтрализация щелочных сточных вод дымовыми газами.
Для нейтрализации щелочных сточных вод могут быть реализованы аналогичные технологические схемы, но наиболее экономичным методом является нейтрализация с помощью дымовых газов, которые образуются в результате сжигания топлива практически на любом производстве.
Дымовые газы содержат в своем составе кислотные оксиды, такие как CO2, SO2, NO, NO2 и др., которые легко вступают в реакции нейтрализации.
Использование дымовых газов позволяет одновременно решить две задачи: нейтрализовать сточные воды и снизить выбросы вредных веществ в атмосферу.
Технологически процесс может быть реализован в разных вариантах, например, в реакторе с импеллерной мешалкой (рис. 2.42) или в скруббере той или иной конструкции (рис. 2.43).
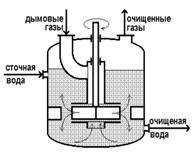
Рис. 2.42. Реактор с импеллерной мешалкой
С точки зрения технологии в первом варианте сплошной фазой является жидкость (сточная вода), а дисперсной – дымовые газы, во втором варианте сплошной фазой являются дымовые газы, дисперсной – сточная вода.
С экономической точки зрения первый вариант более производительный, но и более энергоемкий, второй вариант не требует больших эксплуатационных расходов, но требует громоздкого и металлоемкого оборудования.
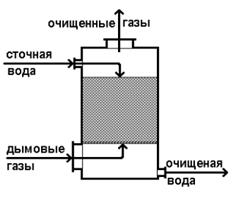
Рис. 2.43. Насадочный скруббер
Дата добавления: 2015-05-07 ; Просмотров: 3715 ; Нарушение авторских прав? ;
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Нейтрализация
Сточные воды нейтрализуются при их химическом взаимодействии с веществами. Производственные сточные воды многих предприятий с повышенным содержанием кислот или щелочей нельзя спускать в канализационную сеть, на очистные станции и в водоемы без предварительного доведения концентрации этих загрязнений до допустимых значений. К таким производственным сточным водам относятся воды химических, машиностроительных, металлургических и нефтеперерабатывающих заводов и особенно тех заводов, где имеются гальванические и термические цехи.
Существует несколько способов нейтрализации производственных сточных вод:
а) непосредственное смешение кислых стоков со щелочными перед спуском их в канализационные сети;
б) использование активной щелочности городских сточных вод или водоема;
в) добавление реагента в пропорциях, необходимых для нейтрализации;
г) фильтрация загрязненных вод через нейтрализующие материалы.
Наиболее часто встречаются производственные сточные воды с повышенной кислотностью, которые сильно воздействуют на материалы труб и отрицательно влияют на микробиальные процессы, происходящие на станциях аэрации. В производственных сточных водах могут содержаться сильные кислоты (первой группы), кальциевые соли которых хорошо растворимы в воде ( HCI , HNO3); сильные кислоты (второй группы), кальциевые соли которых трудно растворимы в воде (H2S04, H2S03), и слабые кислоты (СО2СН3СООН—уксусная).
Нейтрализация сильных кислот первой группы не представляет затруднений, так как образующие их соли растворимы в воде и никакого осадка не дают. Сильные кислоты второй группы нейтрализовать значительно сложнее, так как в осадок выпадает большое количество солей, например гипс CaS04 при нейтрализации серной кислоты. Кроме того, гипс отлагается на поверхности нейтрализующего материала и тормозит процесс реакции.
Если производственные сточные воды поступают в сеть неравномерно и в небольших количествах, то кислые стоки смешивают со щелочными. При этом в некоторые часы суток поступают преимущественно щелочные воды, а в другие часы суток — кислые воды. Для перемешивания таких сточных вод строят специальные резервуары-усреднители для взаимной нейтрализации сточных вод.
Нейтрализацию добавлением реагента проводят тогда, когда смешение стоков и использование активной щелочности водоема не дают желательных результатов, т. е. сточная вода остается кислой.
Для нейтрализации кислот применяют едкий натр, едкое кали, известь, известняк, доломит, мрамор, мел, магнезит, соду, отходы щелочей и пр. Чаще всего используют гидроокись кальция (гашеная известь). Для нейтрализации щелочных сточных вод используют серную, соляную, азотную и другие кислоты.
Реагент можно добавлять в виде раствора (способ мокрого дозирования) или в виде сухого порошка (способ сухого дозирования). Оба эти способа чаще всего применяют для нейтрализации серной кислоты. При пропускной способности установки до 4—5 т/сут нейтрализуемой кислоты выгоднее использовать мокрое дозирование, при большей пропускной способности — сухое. При мокром дозировании реагентом служит известковое молоко, которое приготовляют из обычной товарной извести, подвергнув ее дроблению и гашению в специальных аппаратах. Из этих аппаратов известковое молоко подается насосами в растворные баки, разводится до необходимой концентрации и через дозировочные баки направляется в смеситель, расположенный в канале, по которому движется очищаемая сточная вода. Контакт реагента со сточной водой, необходимый для завершения реакции, осуществляется в специальных резервуарах-нейтрализаторах, рассчитанных на 10—15-минутное пребывание в них жидкости. Нейтрализатор может быть совмещен с отстойником.
Принципиальная схема нейтрализационной установки показана на рис. 1. В состав сооружений входят резервуары-усреднители кислых и щелочных стоков, аппараты для гашения извести, склад негашеной извести, растворные баки, дозаторы, нейтрализаторы, отстойники и сооружения для обезвоживания осадков.
Схема известкового хозяйства при сухом способе хранения извести показана на рис. 13.2. Известь разгружается в приемный бункер и с помощью пластинчатого питателя подается на транспортер, а затем в дробилку. Известковое молоко поступает в резервуар, откуда перекачивается насосами в расходные резервуары. Дозирование извести производится с помощью автоматического дозатора в зависимости от рН обрабатываемой воды.
Для нейтрализации кислых вод можно использовать также отходы местного производства, в частности, шлам из цеха химической водоочистки ТЭЦ. Подобного рода установки применяют для нейтрализации сточных вод травильных цехов заводов черной металлургии.


Нейтрализация фильтрацией заключается в том, что сточную жидкость пропускают через слой фильтрующего материала. При прохождении жидкости через такой фильтр реакция нейтрализации должна полностью заканчиваться. В качестве фильтрующего материала для нейтрализации кислот применяют известняк, мрамор и доломит. Этот способ имеет ряд преимуществ: он более прост и дешев, эффективен при неравномерной концентрации кислот в сточных водах.
Окисление. Этот метод используют в том случае, когда другими методами очистки, в том числе и биохимическим, не удается разрушить или удалить вредные вещества, содержащиеся в производственных сточных водах. Например, сточные воды обогатительных фабрик часто содержат цианистые соединения. Для обработки этих вод применим метод химического окисления путем введения в воду гипохлорита. В качестве реагентов используют гипохлорит кальция, гипохлорит натрия или хлорную известь. Комплекс сооружений для очистки сточных вод окислением представляет собой реагентное хозяйство, которое состоит из склада реагентов, растворных баков и дозаторов, камеры реакций и отстойников.
Применяется также электрохимическая обработка производственных сточных вод. При электрохимической обработке сточных вод проводят анодное окисление, катодное восстановление растворенных загрязняющих веществ, электрокоагуляцию или электродиализ. При такой обработке токсичные вещества превращаются в нетоксичные или малотоксичные. При электродиализе из сточных вод удаляются соли, кислоты или щелочи, которые могут регенерироваться. При электрохимической обработке производственных сточных вод, содержащих цианиды, амины, спирты, азокрасители и пр., происходит их анодное окисление.
При электролизе на катоде выделяется газообразный врдород и разряжаются растворенные в воде ионы металлов. На аноде выделяются кислород и галогены, окисляются некоторые ионы и молекулы с образованием других ионов и молекул. Аноды из железа и алюминия под действием постоянного электрического тока растворяются с образованием оксигидратов и основных солей металлов, способных к коагуляции.
Эффект очистки зависит от состава сточных вод, применяемых материалов для электродов, плотности тока и пр. Применение электрохимических методов целесообразно при относительно высокой электропроводности сточных вод.


Наибольшее распространение получила электрокоагуляция с применением анодов из листового железа и алюминия. Электрокоагуляция применяется, например, при очистке сточных вод гальванических производств, содержащих шестивалентный хром и ионы тяжелых металлов (медь, никель, цинк и др.). Сточные воды (рис. 3) обрабатываются в проточных электролизерах со стальными электродами и горизонтальным или вертикальным движением воды. При электролизе происходит химическое восстановление хромат- и бихроматионов ионами двухвалентного железа, образующимися при растворении стальных анодов. Образуется также гидроокись хрома, железа и других тяжелых металлов.
Перспективной является обработка сточных вод озонированием, позволяющим осуществить глубокую очистку и использовать воды повторно в производстве. В процессе обработки сточной воды озон, подаваемый в реактор в виде озоновоздушной смеси, диспергированной на мельчайшие пузырьки, вступает в химические реакции. Озон получается путем синтеза кислорода воздуха под действием электрического разряда.
Принципиальная технологическая схема озонаторной установки приведена на рис. 4. Она состоит из узла получения озона и узла очистки сточных вод. Узел получения озона в свою очередь состоит из блока очистки и осушки воздуха и блока получения озона. В первом блоке воздух проходит теплообменник, влагоотделитель, фильтр и осушительную установку. Затем воздух поступает в генератор озона. Сточная вода, прошедшая биологическую очистку, подается в реакторы, в которые поступает также озонированный воздух, и проходит процесс окисления.






